文章內容
自己在家做醫生? 微機電系統於居家健康檢測的趨勢
因應未來個人化居家照護之醫療需求,微機電技術運用於微分析系統已成為發展中的重要科技。
隨著科技日新月異、醫療設備快速發展且食物豐沛,人類平均壽命得已延長,全球即將進入老齡化的社會。而在臺灣,除了老齡化社會的到來,醫療人員也面臨嚴重不足的問題。由臺灣近年來死亡原因統計(資料來源:行政院衛生署)可看出,國人十大死因第一位為惡性腫瘤,其次為心血管疾病及其併發症,肺部、肝部疾病,而其中四項又與心血管疾病或其併發症相關。除此之外,由於臺灣外食人口眾多,導致患有三高(高血壓、高血脂及高血糖)的人數比例近年來也大幅提升,並有年輕化的趨勢。因此,血糖、血壓及血脂的監控對於此類慢性病患者是非常重要的,這些患者每週需量測約四次血糖,藉由觀察身體的血糖濃度來控制糖分的攝取,減少併發症的發生。
不論是疾病或者血糖、血脂的檢測方式,都有個共通點,就是大多需要藉由量測血液中待測物(特定分子)的濃度來判斷。然而,在傳統醫院執行檢測前需要先將血液分離及細胞培養才可進行檢測,過程相當耗時,因此大多數患者得在看診前一周或數周前先至醫院進行抽血檢查,才能回診。這樣的流程除了花費許多人力、物力外,大量的人員進出醫院也容易造成疾病交互傳染,若檢測方法對於急性併發症或疾病無法達到及時發現的效果,將可能延誤病患治療的黃金時間,甚至喪失治癒的機會。
因此,致力於研發可應用在居家照顧(point of care)的醫療檢測機台,除了能減少出入醫院的頻率以抑制疾病傳遞的風險外,也能更有效地協助病患自我追蹤且控制疾病。為了達到此目的,許多研究團隊希望利用微機電系統(MEMS)科技達成實驗室晶片(lab on a chip)技術,此一晶片能包含數個機制進行一個或多個血液檢測,如:全血分離、提升待測物濃度及檢測等,以完成醫療檢測機台微型化及居家化的目標,例如「血糖儀」即為已廣受使用的居家檢測機台。
❐現今的生醫檢測技術
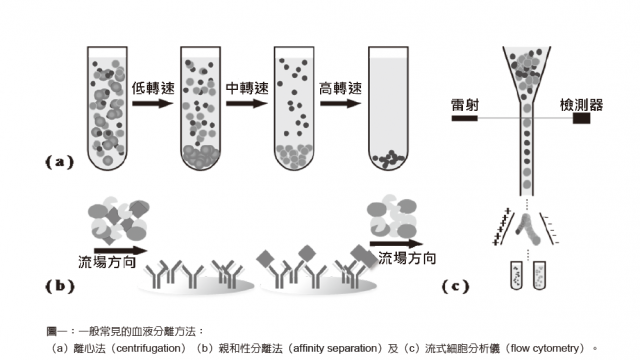
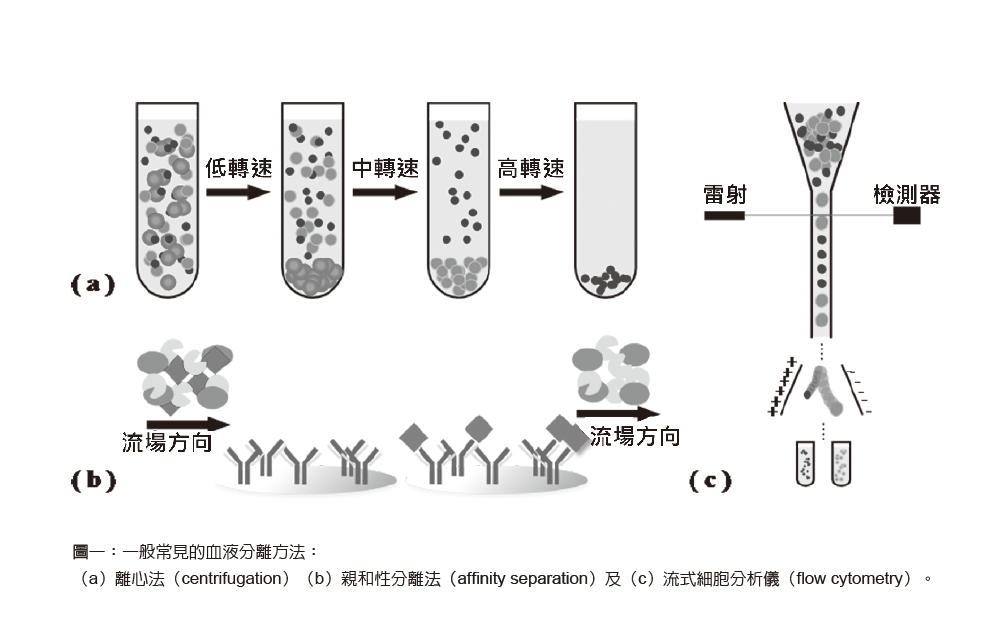
為了達到居家照護的目標,現今醫院的生醫檢測系統是必須被了解的,如:離心法(centrifugation)、親和性分離法(affinity separation)及流式細胞分析儀(flow cytometry)被廣泛應用於血液的分離;利用聚合酶鏈式反應(polymerase chain reaction, PCR)放大基因數量以複製基因,及現今廣泛應用於疾病檢測系統的酵素連結免疫吸附分析法(enzyme-linked immunosorbent assay, ELISA)等。
(一)血液的分離
在生醫檢測系統中,如何將想要的細胞從血液中分離是一個非常重要的課題,由於細胞或生物樣品在血液中的數量非常少,所以如何由血液中正確取出細胞並且在過程中維持其細胞活性就變得相當關鍵。目前實驗室或醫學中心廣泛應用的血液分離方法為離心法(圖一a),它是將存有細胞懸浮液的離心管,利用高速旋轉所產生的離心力分離細胞。由於每種細胞的密度、形狀及大小都不相同,受到離心力作用時所產生的沉澱速度也不相同,故利用此特性來分離細胞,而進行離心時,細胞懸浮液的密度、離心速度及時間都是需要考慮的重要因素。
另外,也有利用將抗體修飾於基板表面,當血液經過這些表面時,由於抗體與抗原擁有專一性鍵結的特性,故只有特定的抗原或細胞才會被黏著於基板表面,當分離完後再利用物理震盪或酵素消化基質等方式取出我們想要的細胞或是生物分子,此種方法稱為親和性分離法(圖一b)。此外,流式細胞分析儀也受到廣泛的應用,它不僅用於分離細胞,也可用來確認細胞的選擇,比如鑑定細胞的標記、分裂週期、DNA含量、細胞凋零(apoptosis)等。其流程為先將含有螢光分子的抗體加入含有細胞的懸浮液中,藉由抗體與抗原的專一性鍵結,使含有螢光分子的抗體與細胞上的抗原連接,再利用管路輸送生物分子並以雷射光激發螢光物質來判別生物分子,此外,再以電場吸引目標的生物分子,達到細胞分離及判斷(圖一c)。
(二)生物分子的檢測
在檢測方面,「聚合酶鏈式反應」是現在不論醫院或者學術界在研究基因時,增加待測基因數量的主要方法。此DNA複製法是由凱利穆利斯(Kary Nullis)發明,他更因此於1993年獲得諾貝爾化學獎。聚合酶鏈式反應的基本原理為對特定的基因做大量的合成,現今的技術可將基因複製為原來的一百億至一千億倍。圖二a為其實驗流程圖,主要分為三個步驟:(1)變性(denaturation),其目的是為了製作出後續要進行DNA複製的模板(template)。由於DNA為雙股螺旋,故利用加熱(約95℃)DNA的方式將雙股DNA拆開成為單股,作為DNA複製的模板;(2)引子黏合(annealing of primers),此步驟是將引子附著於DNA模板的兩端,作為複製DNA的主要基準,雖然引子對於DNA具有專一性的連接,但為了避免引子附著錯誤,在進行時需要控制溫度(如將溫度提高)及時間達到與模板黏合的正確性;(3)引子延長(extension of primers),是利用DNA聚合酶(或稱酵素)使引子延長,現今使用的酵素是於1976年從熱泉中發現的細菌Thermus aquaticus分離出來,它之所以受到廣泛應用的原因在於可耐高溫,便能夠適應PCR反應時的加熱溫度。
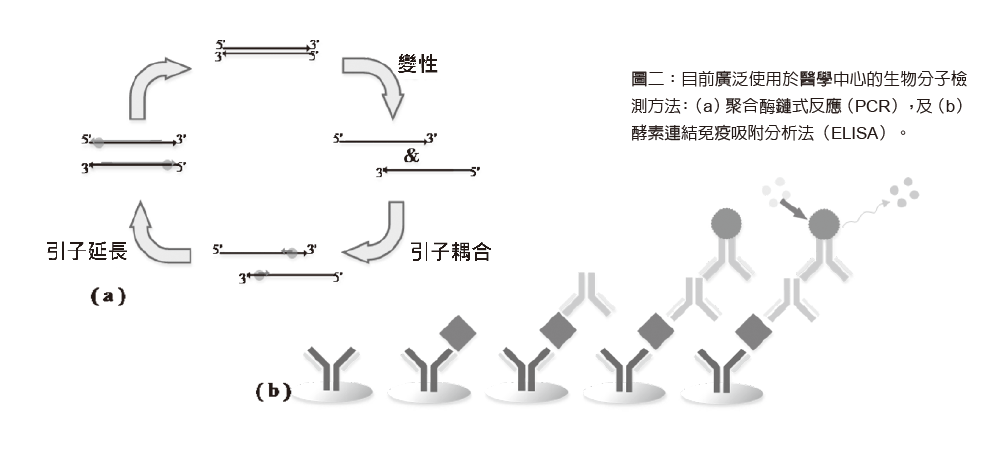
利用這三個步驟循環N次,將可以得到2N個反應產物,大幅增加目標基因的數目,但此循環並非可以無限制的重複,過多的循環也會放大錯誤的產物,過少則目標基因的數目不足,故目前大多重複30~40次。聚合酶鏈式反應除了可以用來作為複製DNA的數量作為診斷工具外,在臨床檢測上也廣受運用。由於PCR可直接鑑別特定的基因是否存在,故可用來偵測基因是否異常,如遺傳性疾病或癌症。此外,由於進行PCR需藉由特定的DNA序列連接,所以也能用來檢測基因的變異,甚至作為刑事案件的血液檢測或血緣關係的鑑定。
另一方面,除了檢測DNA,疾病的檢測也需檢查特定的生物標靶分子(biomarker),如酵素或者蛋白質。一般醫院中,這些生物標靶分子的檢測主要採用的是酵素連結免疫吸附分析法(ELISA)或稱酵素免疫分析法(enzyme-linked immunoassay, EIA)。此方法是以肉眼可見的可見光來確認待測物濃度,檢測原理如(圖二b)所示。ELISA檢測流程以三明治法為例,首先將抗體固定於透明的孔盤上,在洗去未固定於表面之多餘抗體後,加入待測之抗原,使抗體與抗原之間產生專一性鍵結而附著於抗體上;接著,清洗完多餘的抗原後,加入一次抗體與抗原鍵結,反應後洗去未反應之一次抗體;最後,再加入帶有酵素(以horseradish peroxidase為例,簡稱HRP)的二次抗體與一次抗體鍵結,並洗去未反應的二次抗體後,加入TMB與二次抗體上方的HRP產生呈色反應,藉由量測呈色結果即可確定待測抗原的濃度。此方法由於需要兩種抗體進行專一性鍵結,故準確性非常高。此外,由於呈色變化是藉由HRP酵素催化TMB所致,所以呈色的深淺是由酵素的活性與反應時間來決定,若反應時間越長則顏色越深,也因此能藉由酵素催化反應將訊號放大,這也是ELISA具有高敏感度的原因。然而,呈色深淺是相對的結果,與反應時間具有正相關,不同實驗的反應時間與酵素活性難以精確控制,所以在做定量量測時,需要同時檢測不同已知濃度的待測物之吸光度標準曲線,以求出未知待測物的濃度。
❐居家照顧醫療檢測機台
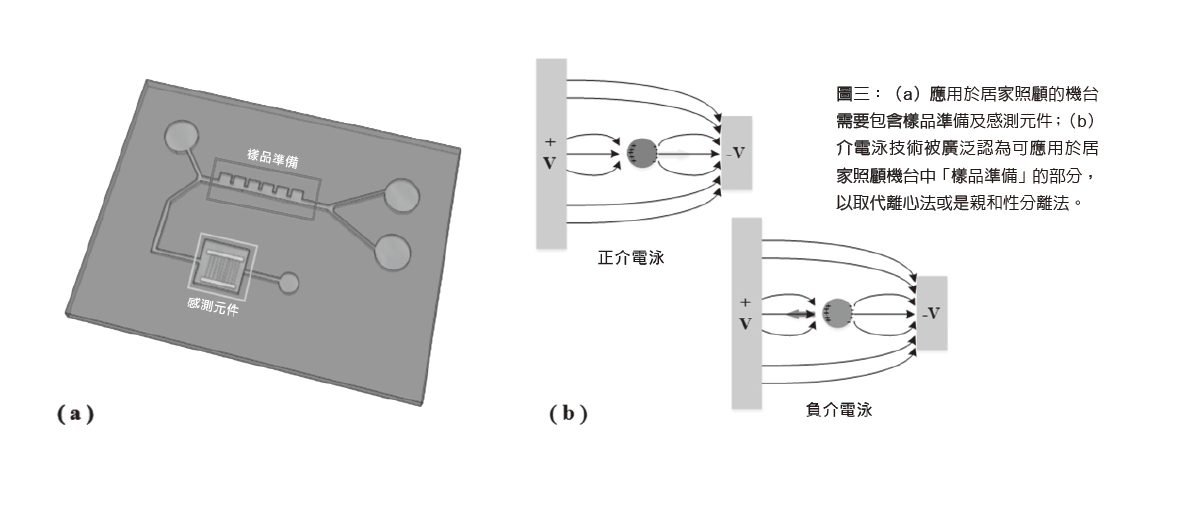
上述的生醫檢測技術,雖然可有效放大待測基因或者準確檢測待測抗原的濃度,但由於操作複雜,待測物的取得流程相當繁瑣,且現行操作機台不易微小化,故無法應用於居家照顧系統上,所以檢測機台的縮小及易於操作是非常重要的。在居家照顧的機台內部需求主要分為兩個區塊:樣品準備及感測元件(圖三a)。
(一)樣品準備
樣品準備可類比為前面所述的離心法、親和力分離法或流式細胞分析儀等,主要功能即為將檢體內的標的細胞分離出來,但為了達到居家照護的需求,前述的三種機制都無法微縮現有的機台,故許多研究希望能利用微機電製程製作出體積小且可以達到分離效果的元件,其中又以介電泳(dielectrophoresis, DEP)式的細胞分離晶片近年來最被廣為研究。
在說明介電泳技術前,我們得先瞭解電泳法(electrophoresis)。電泳,是指帶電粒子在電場作用下向帶有反向電性的電極移動的現象;而「介電泳」是指當外加非均勻電場時,電中性之介電質粒子(一種材料為非良導體,但其特性會受到電場影響的材料)會受到電場的作用產生極化(polarization)現象,而介電質粒子會在極化作用下產生偶極(dipole),並隨著空間中電場強度的變動產生介電泳力(dielectrophoresis force),使得介電質粒子往電場強的區域聚集。介電質粒子往高電場的方向移動稱為正介電泳;反之,為負介電泳。而由於介電泳力會受到介電質粒子的特性或外加電場所影響,所以就能利用細胞或生物分子表面電荷、大小或形狀的差異,或者控制電場梯度的分布,使細胞產生不同的移動,進而分離細胞了(圖三b)。
(二)感測元件
居家照護所需的檢測機台,另一個重要的部分為樣品的檢測,目前醫院所利用的方法為酵素連結免疫吸附分析法,但此法耗時且操作人員必須受過專業訓練,故無法應用於居家照顧系統上。為了擁有一個可以應用於居家照顧的檢測晶片,這樣的元件必須擁有體積小、成本低、容易操作及判別的優點,而今微機電技術純熟,對於生醫檢測晶片的發展是不可或缺的助力,因此各式各樣的微機電生醫檢測晶片研發正如火如荼的進行,如:電化學(electrochemistry)檢測、微懸臂樑(microcantilever)檢測、奈米線電晶體(nanowire transistor)檢測等。
(1)微懸臂樑結構
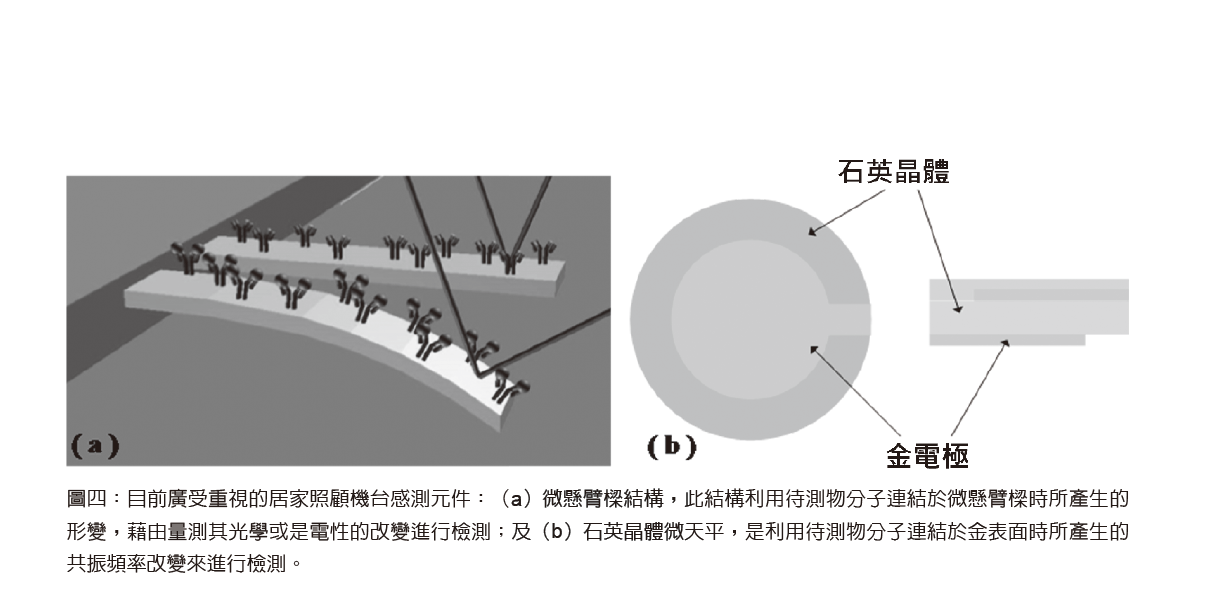
微機電生醫晶片中,其中一項非常受到重視的領域為利用微懸臂樑結構製作生醫檢測元件。微懸臂樑為一端固定、另一端懸浮的微型結構(圖四a),利用它「共振頻率」或「表面應力」的改變做為檢測的機制。由於理想的微懸臂樑結構會有一個共振的頻率,此頻率與材料的勁度呈根號正比關係,也與微懸臂樑質量呈根號反比,當生物分子或待測物質鍵結於微懸臂樑表面時,將使得微懸臂樑質量改變,導致微懸臂樑感測器產生共振頻率之變化,利用此變化就可測量生物分子或待測物質的濃度。
以相同的微懸臂樑結構,另一種方式是利用表面應力的改變進行檢測。應力是指單位面積下所承受的作用力,當微懸臂樑表面產生變化時,如與生物分子連結或反應,將會造成微懸臂樑表面應力改變,此不對稱的應力將會造成微懸臂樑受到張應力(tensile stress)或者壓應力(compressive stress),因此讓微懸臂樑往下或往上彎曲,故藉由分析微懸臂樑受到的表面應力的變化量(如:光學或壓阻),便可得知微懸臂樑的變形量,進而分析生物分子或待測物在微懸臂樑表面的連結量或是反應狀況。
例如光學式微懸臂樑,是將雷射光束聚集於微懸臂樑結構之尖端,當生物分子或待測物連結於微懸臂樑表面使得微懸臂樑產生彎曲時,雷射光所反射的位置會產生位移的現象,利用光學感測器記錄反射光位移量的變化即可分析出待測物的反應或連結狀況;另一種檢測方法是利用材料本身的壓阻效應,壓阻效應是指當材料受到機械式應力產生形變時會改變材料的阻抗(電荷在材料中傳遞受到的阻力),故當生物分子或待測物連結於微懸臂樑表面導致微懸臂樑彎曲形變時,微懸臂量的阻抗將會改變,量測微懸臂樑元件阻抗的變化,也可了解待測物的反應或連結狀況。
(2)石英晶體微天平
有別於微懸臂樑結構可利用各種力、光及電等物理特性的改變作為生醫檢測的依據,另一個生醫檢測元件則是利用壓電效應。壓電效應是指以壓電材料(介電質材料)將外加的機械能與電能產生轉換的作用,壓電材料可分為正壓電材料(direct piezoelectric material)及逆壓電材料(converse piezoelectric material)。施加壓力於壓電材料時,其可將形變的機械能轉換成電能稱之為正壓電效應;逆壓電效應則是指外加電場於壓電材料時使其產生形變的現象。石英晶體微天平(quartz crystal microbalance, QCM)便是將逆壓電效應運用於生醫檢測之中(圖四b)。當施加交流電壓於石英晶體微天平時,逆壓電效應會使石英晶體產生簡諧振盪,當外加的交流電壓與石英晶體微天平的頻率一致時,石英晶體微天平會產生最大的振幅,此時的頻率則為共振頻率,當生物分子或是待測物質與石英晶體微天平連結或反應時,會改變共振頻率,利用此變化就能推測生物分子或是待測物質連結於石英晶體微天平的含量。
❐總結
因應人口老化所需要的居家照顧檢測系統是未來重要的科技發展方向,利用居家檢測系統也可減少疑似病患到醫院做檢查,如此不但能大量降低醫療院所的負擔及社會成本,同時也可減少傳染性疾病快速散播。為了完成適合於居家照顧的檢測系統,使檢測機台微小化即成為一項重要的研究。由於半導體技術及微機電技術可以達到體積小、成本低及大量製程的優點,故可以利用介電泳作為血液的分離,以微懸臂樑結構、石英晶體微天平,甚至是奈米線電晶體等方法作為疾病檢測的結構,製作出實驗室晶片以滿足未來居家照顧的需求,進而達到慢性疾病的控制,因此,眾多研究學者正積極發展微分析系統相關技術,以期對未來社會創造更多的福祉。
陳柏翰:任職臺灣大學電子工程學研究所
薛孝庭:任職臺灣大學生醫電子與資訊學研究所
林致廷:任職臺灣大學電子工程學研究所/生醫電子與資訊學研究所
【延伸閱讀】其他精彩內容請線上訂閱「科學月刊」。<我要訂閱>
1. Murray R. K. et al., Harper’s Illustrated Biochemistry, New York, McGraw-Hill, 2003.
2. Wu, G. et al., Bioassay of prostate-specific antigen (PSA) using microcantilevers, Nature Biotechnology, Vol. 19: 856-860, 2001.
3. Janshoff, A. and Steinem, C., Piezoelectric Sensors, Berlin, Springer, 2007.
